Chapter-3. परमाणु एवं अणु Science class 9 in hindi Medium CBSE Notes
CBSE Class 9 Science Notes in Hindi Medium based on latest NCERT syllabus, covering definitions, diagrams, formulas, and exam-oriented explanations.

3. परमाणु एवं अणु
सरल यौगिकों का निर्माण
रासायनिक सूत्र लिखते समय निम्न नियमों का पालन करे :
(i) आयन की संयोजकता अथवा आवेश संतुलित होना चाहिए।
(ii) जब एक यौगिक किसी धातु एवं अधातु के संयोग से निर्मित होता है तो धातु के नाम अथवा उसके प्रतीक को रासायनिक सूत्रा में पहले लिखते हैं। उदाहरणार्थः कैल्सियम आॅक्साइड
(CaO) सोडियम क्लोराइड (NaCl) आयरन सल्फाइड (FeS) काॅपर आॅक्साइड (CuO) इत्यादि|
(iii) आॅक्सीजन, क्लोरीन, सल्फर अधातुयें हैं तथा उन्हें दायीं तरफ लिखते हैं, जबकि कैल्सियम, सोडियम, आयरन एवं काॅपर धातुएँ हैं तथा उन्हें बायीं तरपफ लिखते हैं।
(iv) बहुपरमाणुक आयनों द्वारा निर्मित यौगिकों में आयन को पहले कोष्ठक में रखते हैं। तत्पश्चात् अनुपातों को दर्शाने वाली संख्या को लिखते हैं।
द्विअंगी यौगिक: दो भिन्न-भिन्न तत्वों से निर्मित सरलतम यौगिकों को द्विअंगी यौगिक कहते हैं |
सरल यौगिकों के सूत्र लिखना:
आण्विक यौगिकों के रासायनिक सूत्र लिखते समय हम पहले संघटक तत्वों के प्रतीक लिखकर
उनकी संयोजकताएँ लिखते हैं तत्पश्चात् संयोजित परमाणुओं की संयोजकताओं को क्राॅस करके (cross over) अणु सूत्र लिखते हैं।
यहाँ अणु में भाग लेने वाले दोनों तत्व अधातु हैं |
उदाहरण 1:
हाइड्रोजन क्लोराइड का सूत्र:
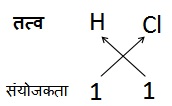
अत: सूत्र : HCl
उदाहरण 2:
हाइड्रोजन सल्फाईड़ का सूत्र:

उदाहरण 3:
कार्बन टेट्राक्लोराइड का सूत्र:

अत: सूत्र : CCl4
आयनिक यौगिकों का सूत्र (Formula of Ionic Compound): इसमें पहला तत्व धातु होता है जो धनायन (cation) बनाता है और दूसरा तत्व अधातु होता है जो ऋणायन (anion) बनाता है |
मैग्नीशियम क्लोराइड का सूत्र:
मैग्नीशियम क्लोराइड का सूत्र ज्ञात करने के लिए पहले हम धनायन का संकेत (Mg+) लिखते हैं इसके पश्चात् ऋणायन क्लोराइड (Cl-) लिखते हैं। तत्पश्चात् इनके आवेशों को आड़ा-तिरछा (criss-cross) करके हम सूत्र प्राप्त करते हैं।
उदाहरण 4:

अत: सूत्र : MgCl2
उदाहरण 5:
ऐलुमिनियम ऑक्साइड का सूत्र:

अत: सूत्र : Al2O3
बहुपरमाणुक आयनों वाले यौगिक:
उदाहरण 6:
सोडियम नाइट्रेट का सूत्र:

अत: सूत्र : NaNO3
उदाहरण 6:

अत: सूत्र : (NH4)2SO4
आण्विक द्रव्यमान (Molecular Mass):
किसी पदार्थ का आण्विक द्रव्यमान उसके सभी संघटक परमाणुओं के द्रव्यमानों का योग होता है। जैसे- जल (H2O) का आण्विक द्रव्यमान
हाइड्रोजन का परमाणु द्रव्यमान = 1 u
ऑक्सीजन का परमाणु द्रव्यमान = 16 u
जल के अणु में हाइड्रोजन के 2 अणु है और ऑक्सीजन के 1 अणु है
∴ जल का आण्विक द्रव्यमान = 2 x 1 + 16 = 18 u
इस प्रकार यह अणु का वह सापेक्ष द्रव्यमान है जिसे परमाणु द्रव्यमान इकाई (u) द्वारा व्यक्त किया जाता है।
सूत्र इकाई द्रव्यमान (Formula Unit Mass):
किसी पदार्थ का सूत्र इकाई द्रव्यमान उसके सभी संघटक परमाणुओं के परमाणु द्रव्यमानों का योग होता है। सूत्र द्रव्यमान का उपयोग तब करते हैं जब पदार्थ का संघटक आयन हों |
जैसे -
NaCl, CaCl2, Al2O3, MgCl2 आदि |
सूत्र द्रव्यमान का परिकलन उसी प्रकार से करते हैं जिस प्रकार से हमने आण्विक द्रव्यमान का परिकलन किया है। अंतर केवल इतना होता है कि यहाँ पर हम उस पदार्थ के लिए सूत्र इकाई का उपयोग करते हैं, जिसके संघटक आयन होते हैं।
- किसी पदार्थ की मात्रा उसके द्रव्यमान से अथवा उसके परमाणुओं की संख्या से अभिलक्षित कर सकते हैं।
मोल (Mole):
मोल पदार्थ की वह मात्रा है जिसमें कणों की संख्या (परमाणु, आयन, अणु या सूत्र इकाई इत्यादि) कार्बन-12 के ठीक 12 g में विद्यमान परमाणुओं के बराबर होती है। वह मात्रा उस पदार्थ का एक मोल कहलाता है |
मोल एक प्रकार से बहुत सारे परमाणुओं का ढेर (heap) है | जिसमें' किसी भी तत्व के परमाणुओं, अणुओं अथवा आयनों की संख्या 6.022 x 1023 होता है |
आवोगाद्रो संख्या आवोगाद्रो स्थिरांक: किसी पदार्थ के एक मोल में कणों (परमाणु, अणु अथवा आयन) की संख्या निश्चित होती है | जिसका मान 6.022 x 1023 होता है | इसी संख्या को आवोगाद्रो स्थिरांक या आवोगाद्रो संख्या कहते हैं |
जैसे -
| तत्व के परमाणु | परमाणु द्रव्यमान (u) | मात्रा (g) में | मोलों की संख्या | परमाणुओं की संख्या |
| हाइड्रोजन | 1 u | 1 g | 1 | 6.022 x 1023 |
| कार्बन | 12 u | 12 g | 1 | 6.022 x 1023 |
| नाइट्रोजन | 14 u | 14 g | 1 | 6.022 x 1023 |
| ऑक्सीजन | 16 u | 16 g | 1 | 6.022 x 1023 |
| सोडियम | 23 u | 23 g | 1 | 6.022 x 1023 |
तालिका को देखें और निम्न बातों को समझें :
-- हाइड्रोजन का 1 g परमाणु में 1 मोल होता है और उस 1 मोल में परमाणुओं की संख्या 6.022 x 1023 होती है |
-- कार्बन का 12 g परमाणु में 1 मोल होता है और उस 1 मोल में परमाणुओं की संख्या 6.022 x 1023 होती है |
-- ऑक्सीजन के 16 g परमाणु में 1 मोल होता है और उस 1 मोल में ऑक्सीजन परमाणुओं की संख्या 6.022 x 1023 होती है |
इसी प्रकार आप सभी परमाणु का मोल ज्ञात कर सकते है और उसमें परमाणुओं की संख्या ज्ञात कर सकते हैं |
अब इसे समझे :
-- हाइड्रोजन के 1 u में 1 परमाणु होता है |
-- कार्बन के 12 u में भी 1 परमाणु होता है |
-- नाइट्रोजन के 14 u में भी 1 परमाणु होता है |
-- ऑक्सीजन के 16 u में भी 1 परमाणु होता है |
इसी प्रकार आप सभी तत्वों के परमाणुओं का भी ज्ञात कर सकते हैं |
मोलर द्रव्यमान (Molar mass): किसी तत्व के परमाणुओं के एक मोल का द्रव्यमान को मोलर द्रव्यमान कहते है | परमाणुओं के मोलर द्रव्यमान को ग्राम परमाणु द्रव्यमान भी कहते हैं |
उदाहरण:
हाइड्रोजन के एक परमाणु का द्रव्यमान = 1 u
अत: हाइड्रोजन का ग्राम परमाणु द्रव्यमान = 1 g होगा, और 1 g हाइड्रोजन में हाइड्रोजन के 1 मोल परमाणु होते है और इस 1 मोल में हाइड्रोजन परमाणुओं की संख्या 6.022 x 1023 होता है |
इसी प्रकार कार्बन के 1 मोल का मोलर द्रव्यमान 12 g है |
ऑक्सीजन के 1 मोल का मोलर द्रव्यमान 16 g है |
सोडियम के 1 मोल का मोलर द्रव्यमान 23 g है |
इसीप्रकार:
1 u हाइड्रोजन में केवल 1 हाइड्रोजन परमाणु होता है |
4 u हीलियम में केवल 1 हीलियम परमाणु होता है |
12 u कार्बन में केवल 1 कार्बन परमाणु होता है |
इस पाठ के अन्य दुसरे विषय भी देखे :
Class 9, all subjects CBSE Notes in hindi medium, cbse class 9 Science notes, class 9 Science notes hindi medium, cbse 9 Science cbse notes, class 9 Science revision notes, cbse class 9 Science study material, ncert class 9 science notes pdf, class 9 science exam preparation, cbse class 9 physics chemistry biology notes
 Welcome to ATP Education
Welcome to ATP Education
 ATP Education
ATP Education