Chapter-3. परमाणु एवं अणु Science class 9 in hindi Medium CBSE Notes
CBSE Class 9 Science Notes in Hindi Medium based on latest NCERT syllabus, covering definitions, diagrams, formulas, and exam-oriented explanations.

3. परमाणु एवं अणु
आयन एवं बहुपरमाणुक आयन
नोट: इस पाठ के अन्य विषय जैसे अणु और आयन का बनना को समझने के लिए सबसे पहले हमें परमाणु के अवपरमाणुक कणों जैसे प्रोट्रांन, न्यूट्रॉन और इलेक्ट्रान के बारे में समझना होगा | इलेक्ट्रॉनो के वितरण (electronic configuration) और संयोजकता (velency) को जानना होगा | वैसे इन विषयों को इस पुस्तक के अध्याय 4 परमाणु की संरचना में पढना है |
किसी भी परमाणु में चाहे वो किसी भी तत्व का परमाणु क्यों न हो सभी में तीन अवपरमाणुक कण होते हैं |
(i) प्रोट्रान: यह धन आवेशित (+) कण होता है जो परमाणु के नाभिक में रहता है | यह तत्व के सभी रासायनिक गुण धर्म को प्रदर्शित करता है | परमाणु में प्रोट्रान के घटने या बढ़ने से उसके रासायनिक गुणधर्म भी बदल जाते हैं |
(ii) इलेक्ट्रान: परमाणु: यह ऋण आवेशित (-) कण है जो नाभिक के चारों ओर भिन्न-भिन्न और निश्चित कक्षाओं में चक्कर काटते हैं |
(iii) न्यूट्रॉन: न्यूट्रॉन परमाणु के नाभिक में उपस्थित बिना आवेश वाला कण है जिस पर कोई आवेश नहीं होता है |
उदासीन परमाणु: समान्यत: कोई भी परमाणु उदासीन होता है क्योंकि परमाणु में धन प्रोट्रानो की संख्या ऋण इलेक्ट्रानों की संख्या के बराबर होता है यही कारण है कि किसी भी परमाणु पर नेट आवेश शून्य होता है और परमाणु उदासीन होता है |
जैसे ऑक्सीजन (O) के परमाणु में 8 धन प्रोट्रान होते है उतनी ही ऋण इलेक्ट्रान होते है |
इलेक्ट्रोनिक विन्यास (Electronic Configuration): किसी परमाणु के विभिन्न कोशों में इलेक्ट्रोनों के वितरण को इलेक्ट्रोनिक विन्यास कहते हैं |
हाइड्रोजन का इलेक्ट्रॉनिक संरचना:
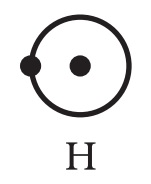
हाइड्रोजन में 1 इलेक्ट्रान होता है अत: इसके बाह्यतम कक्षा K में केवल एक ही इलेक्ट्रान रहता है |
कार्बन के परमाणु का इलेक्ट्रॉनिक संरचना:

कार्बन के पास कुल 6 इलेक्ट्रॉन्स होते है तो इसके सबसे भीतरी कक्षा K में 2 इलेक्ट्रान रहता है और बहरी कक्षा L में शेष बचे 4 इलेक्ट्रॉन्स रहता है |
ये कोश होते हैं :
K, L, M, N आदि
कोश K में अधिकतम 2 इलेक्ट्रॉन्स रह सकते हैं |
कोश L में अधिकतम 8 इलेक्ट्रॉन्स रह सकते हैं |
कोश M में अधिकतम 18 इलेक्ट्रॉन्स रह सकते हैं और
कोश N में अधिकतम 32 इलेक्ट्रॉन्स रह सकते हैं |
कोशों में अधिकतम इलेक्ट्रॉन्स को रखने के लिए एक सूत्र है: 2n2
जिसके आधार अधिकतम इलेक्ट्रॉन्स की संख्या ज्ञात की जाती है :
जैसे पहले कोश K के लिए : 2(1)2 = 2 x 1 = 2
दुसरे कोश L के लिए : 2(2)2 = 2 x 4 = 8
तीसरे कोश M के लिए : 2(3)2 = 2 x 9 = 18
चौथे कोश N के लिए : 2(4)2 = 2 x 16 = 32
संयोकजता (valency): किसी परमाणु के बाह्यतम कक्षा में उपस्थिति संयोजी इलेक्ट्रॉन्स की संख्या को उस तत्व की संयोजकता कहते हैं |
जैसे :
कुछ तत्वों का इलेक्ट्रॉनिक विन्यास और उनकी संयोजकता:
जैसे किसी तत्व के बाह्यतम कक्षा में 1 इलेक्ट्रॉन् है तो उसकी संयोजकता 1 ही होगी | यदि उसके बाह्यतम कक्षा में 2 , 3 या 4 है तो उसकी संयोजकता भी क्रमश: 2, 3 या 4 होगी | यदि बाह्यतम कोश में 5, 6 या 7 इलेक्ट्रॉन्स है तो संयोजकता निम्नानुसार ज्ञात किया जाता है |
जब बाह्यतम कोश में 5 हो तो संयोजकता = 8 - 5 = 3
जब बाह्यतम कोश में 6 हो तो संयोजकता = 8 - 6 = 2
जब बाह्यतम कोश में 7 हो तो संयोजकता = 8 - 7 = 1
जब बाह्यतम कोश में 8 हो तो संयोजकता = 8 - 8 = 0
अब यह तालिका देखिए:
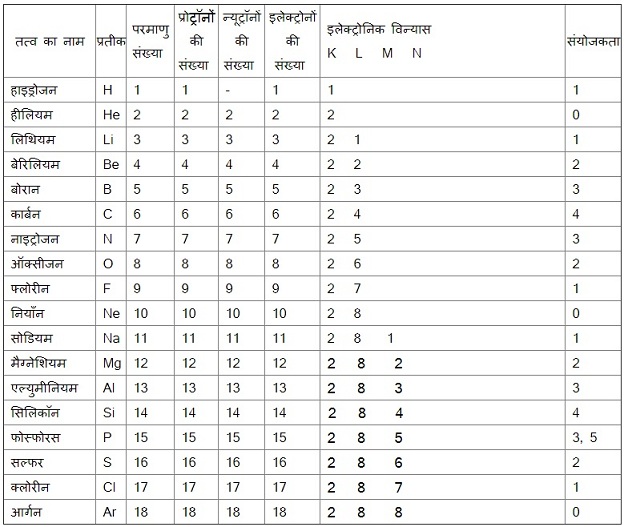
किसी परमाणु के आवेशित कणों को आयन कहते है | आयन:
- धातु एवं अधातु युक्त आवेशित कणों से बने होते है |
- इन आयनों पर ऋण अथवा धन आवेश होता है |
- ऋण आवेशित कण को ऋणायन (anion) तथा धन आवेशित कण को धनायन (cation) कहते है |
- जो तत्व धनायन (cation) बनाते है उनपर (+) का चिन्ह लगा कर दर्शाया जाता है और जो ऋणायन (anion) बनाते है उन पर (-) का चिन्ह लगाया जाता है |
- आयन एक आवेशित परमाणु अथवा परमाणुओं का एक ऐसा समूह होता है
जिस पर नेट आवेश विद्यमान होता है।
बहुपरमाणुक आयन:
परमाणुओं के समूह जिन पर नेट आवेश विद्यमान हो उसे बहुपरमाणुक आयन कहते हैं।
उदाहरण:
N3- + H44+ = NH4+
यहाँ नाइट्रोजन पर 3 ऋण आवेश है और हाइड्रोजन पर 4 धन आवेश है तो कुल नेट आवेश अर्थात शुद्ध आवेश 1 धन (+) प्राप्त होगा | अत: यह अणु एक धन आवेश (+) वाला बहुपरमाणविक आयन बनाएगा |
अमोनियम (Ammonium) NH4+
कार्बोनेट (Carbonate) CO3-
हाइड्रोऑक्साइड (Hydroxide) OH-
नाइट्रेट (Nitrate) NO3-
नाइट्राइट (Nitrite) NO2-
फॉस्फेट (Phosphate) PO43-
सल्फेट (Sulfate) SO42-
सल्फाईट (Sulfite) SO32-
परमाणु तथा आयन में अंतर:
परमाणु:
1. यह विद्युत उदासीन कण होते हैं |परमाणु :
2. इसमें प्रोट्रॉन तथा इलेक्ट्रान बराबर संख्या में होते हैं |
3. अक्रिय गैस को छोड़कर सभी परमाणुओं का इलेक्ट्रोनिक रचनाएँ अस्थायी होते हैं |
4. ये स्वतंत्र रूप से अस्तित्व में नहीं रह सकते हैं |
5. ये आयनिक अभिक्रिया में भाग नहीं लेते हैं |
6. ये अस्तित्व में बने रहने के लिए इलेक्ट्रॉन्स की साझेदारी करते हैं |
आयन:
1. यह विद्युत आवेशित कण होते हैं |
2. इसमें प्रोट्रॉन तथा इलेक्ट्रान बराबर संख्या में नहीं होते हैं |
3. आयनों का इलेक्ट्रोनिक रचनाएँ स्थायी होते हैं |
4. ये स्वतंत्र रूप से अस्तित्व में रह सकते हैं |
5. ये आयनिक अभिक्रिया में भाग लेते हैं |
6. ये अस्तित्व में बने रहने के लिए इलेक्ट्रान को ग्रहण करते है या त्याग करते है |
इस पाठ के अन्य दुसरे विषय भी देखे :
Class 9, all subjects CBSE Notes in hindi medium, cbse class 9 Science notes, class 9 Science notes hindi medium, cbse 9 Science cbse notes, class 9 Science revision notes, cbse class 9 Science study material, ncert class 9 science notes pdf, class 9 science exam preparation, cbse class 9 physics chemistry biology notes
 Welcome to ATP Education
Welcome to ATP Education
 ATP Education
ATP Education